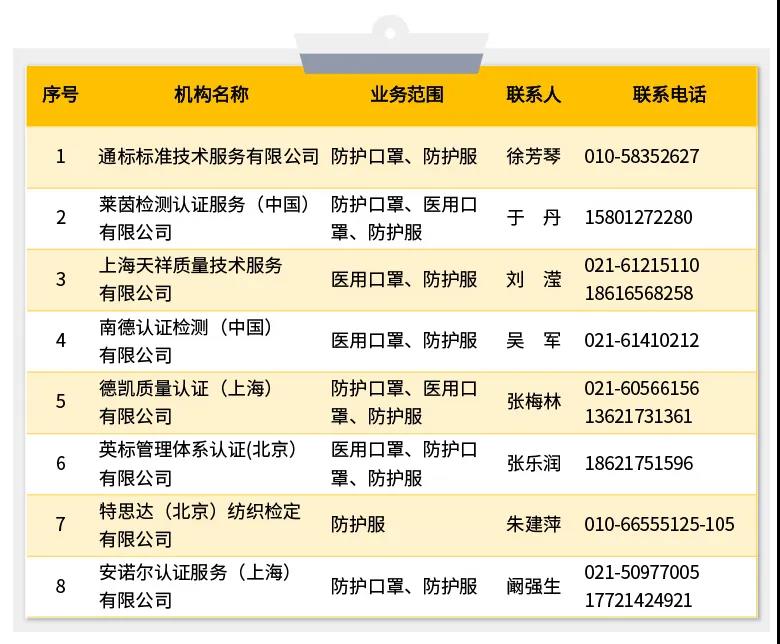
口罩等医疗物资出口海关100%查验,违规将被扣货且巨额罚款!出口欧盟及美国市场认证信息指南!国内具有相应资质能力的认证机...
19个商品编码项下实施出口品质检验
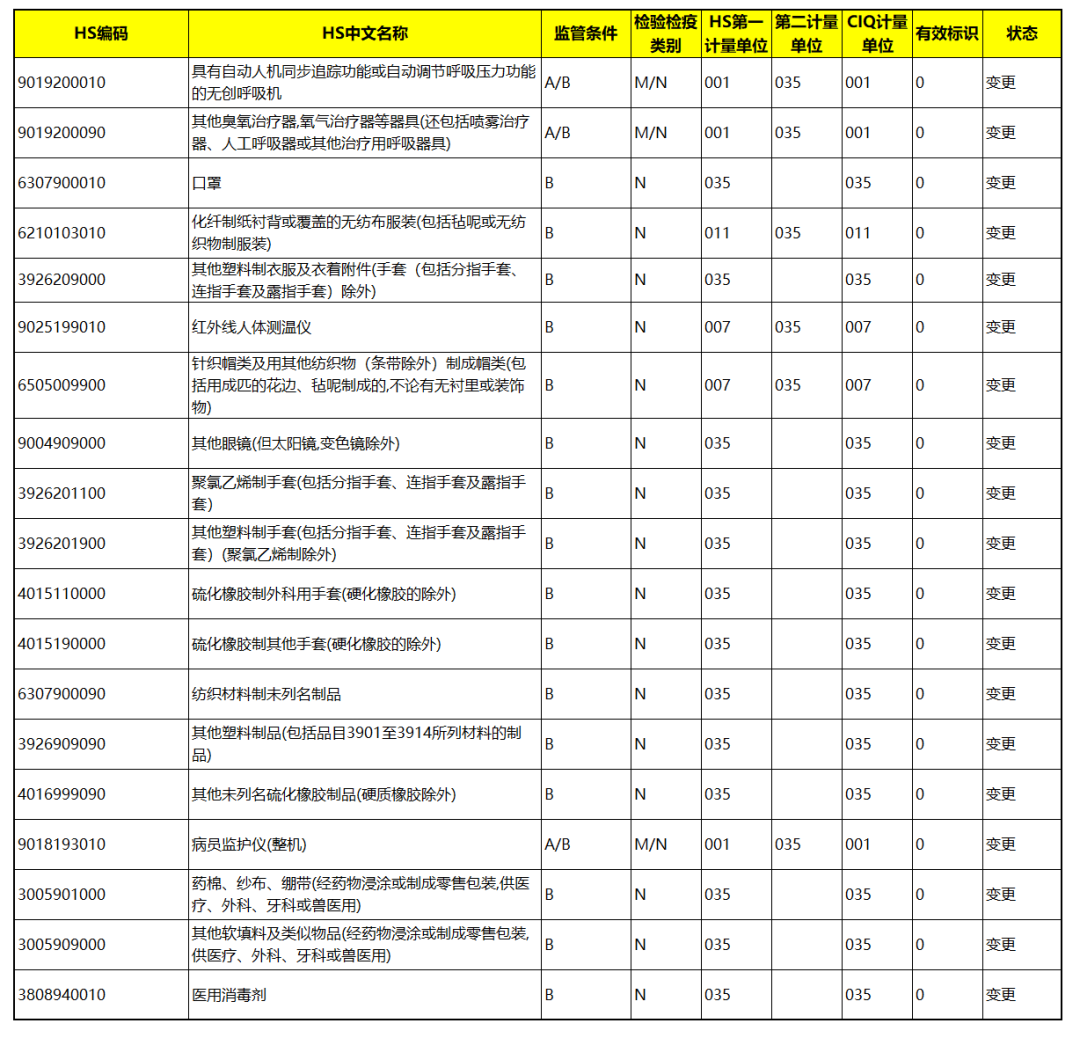
仅供参考,以海关实际发布为准。
自3月31日发布《关于有序开展医疗物资出口的公告》以来,海关在贸易、邮件、快件、跨境电商等渠道,共查获非清单企业生产或无医疗器械产品注册证书的医疗物资1120.5万件,其中口罩994.1万只,防护服15.5万套,新冠病毒检测试剂108.5万份,红外测温仪2.4万件。
现要求出口的新冠病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计等5类产品必须取得国家药品监管部门相关资质,符合进口国(地区)质量标准要求。实施100%单证审核,重点验核品名、数量与申报是否相符,外观是否霉变、有无污染/污化、是否超出保质期、是否破损及侵权,以及是否存在夹藏夹带、掺杂掺假、以假充真、以次充好、以不合格商品冒充合格商品等情况。
★ 夹藏口罩 40500只! ★


海关提醒,为有效支持全球抗击疫情,保证产品质量安全、规范出口秩序,自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。
▼▼▼
KN95为何申报为
“非医疗用无牌无型号一次性口罩”
4月1日,厦门海关所属邮局海关查验关员监管一票出口至意大利的防控物资时,发现货物申报品名为“非医疗用无牌无型号一次性口罩”,但实际货物却为艾美牌KN95、鑫胜康牌KN95,共计4000个,存在伪瞒报情况。

4月2日,该关再次查获出口防疫物资违规情事。一批出口至阿富汗的申报为“非医疗用猫咖牌额温枪”的防疫物资,经开箱后发现其实际品名为“红外额温计”,共计48支,未标注医疗器械产品注册证号码。经核实,该家医疗器械公司并无相关注册在案的额温枪信息。
目前上述货物均按规定进行暂扣,待下一步处置。
相
关
要
求
根据《商务部 海关总署 国家药品监督管理局公告2020年第5号 关于有序开展医疗物资出口的公告》要求,自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。上述医疗物资出口质量监管措施将视疫情发展情况动态调整。
★ 高效防护口罩出口,请走正规渠道 ★


黄埔海关所属老港海关根据布控指令查验时,发现该批货物实际为食品、纸杯等,结合对机检图像的分析研判,现场查验关员在集装箱底部发现夹藏的口罩15.3万个,包括一次性日常防护口罩和一次性高效防护口罩,均具备合格证。目前,海关已将该批货物移交后续处置部门处理。
▼▼▼
对于海关查获的出口医疗物资违法违规行为,将依法依规对涉事企业进行严肃处理:
一是对于以伪瞒报方式逃避海关监管的,海关将依照《海关法》《海关行政处罚实施条例》的规定,没收走私货物及违法所得,可以并处罚款;构成犯罪的,司法机关可依照《刑法》有关规定,视情节处有期徒刑或者拘役,并处或者单处罚金。
二是对于出口医疗物资掺杂掺假、以假充真、以次充好、以不合格商品冒充合格商品的,海关依照《进出口商品检验法》的规定,责令停止出口,没收违法所得,并处货值金额50%以上3倍以下罚款。
三是上述被海关处罚的违法行为将作为海关认定企业信用状况的参考依据。构成走私行为或者走私犯罪的,海关将企业信用等级直接降为失信企业,并实施提高查验比例、加大稽核查频次、全额收取担保金等严格管理措施。同时,海关总署还将与国家有关部门对该企业实施联合惩戒。
四是加大对被处罚企业违法情事的曝光力度,在海关总署官方网站和地方信用网站公开被处罚企业相关信息,并通过媒体曝光有关案件信息。
口罩等防疫用品出口欧盟及美国市场认证信息指南!
电脑端打开网址:
http://www.cnca.gov.cn/xxgk/hydt/202004/t20200404_58016.shtml
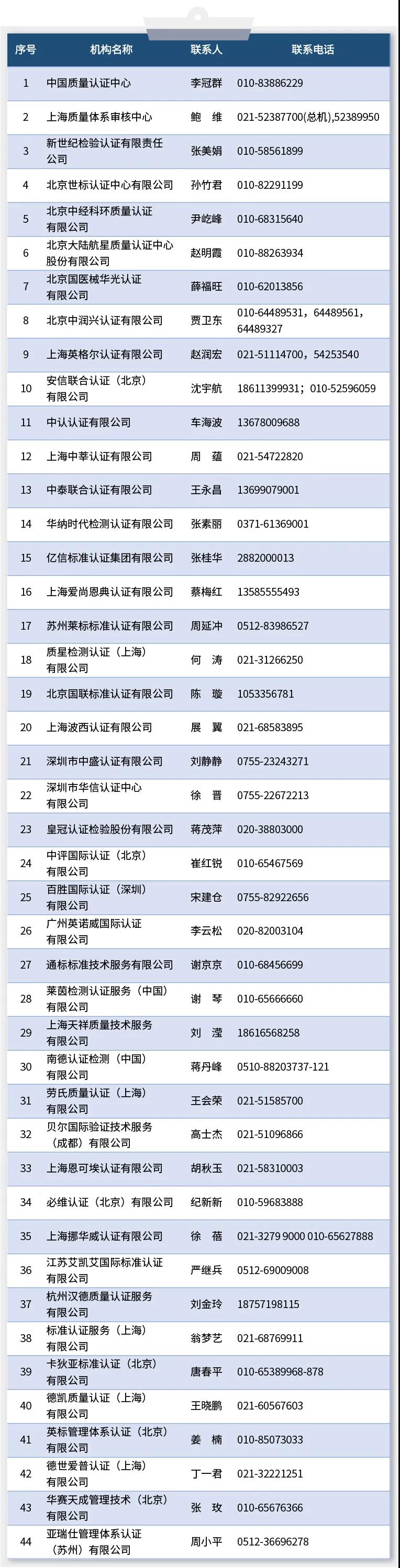
为做好新冠肺炎疫情防控和经济社会发展工作,支持企业复工复产,针对企业不熟悉防疫物资出口政策等实际问题,现就口罩等防疫用品出口欧盟及美国的相关准入要求及梳理的国内具有相应资质能力的认证机构名录提供如下信息指南,供企业参考。
一、欧盟对口罩等防疫用品准入要求
(一)口罩
欧盟根据用途将口罩分为两类:医用口罩和个人防护口罩。
1、医用口罩
医用口罩需按照欧盟医疗器械指令93/42/EEC(MDD)或欧盟医疗器械条例EU2017/745(MDR)加贴CE标志,对应的标准是EN14683。根据口罩产品无菌或非无菌状态,采取的合格评定模式也不同。
(1)无菌医用口罩:必须由授权公告机构进行CE认证。
(2)非无菌医用口罩:企业只需进行CE自我符合性声明,不需要通过公告机构认证。在准备好相应文件及测试报告等资料后,即可自行完成符合性声明。
2. 个人防护口罩
个人防护口罩不属于医疗器械,但需符合欧盟个人防护设备条例EU2016/425(PPE)要求,由授权公告机构进行CE认证并颁发证书,对应的标准是EN149。
(二)防护服
防护服也分为医用防护服和个人防护服,管理要求与口罩基本类似。医用防护服按照医疗器械管理,其中无菌医用防护服需按照欧盟医疗器械指令93/42/EEC(MDD)或欧盟医疗器械条例EU2017/745(MDR)获得CE认证,非无菌医用防护服只需进行CE自我声明。个人防护服需按照欧盟个人防护设备条例EU2016/425(PPE)获得CE认证。
(三) 欧盟公告机构查询地址
1.欧盟医疗器械指令93/42/EEC(MDD)授权的公告机构查询地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13
2.欧盟医疗器械条例EU 2017/745(MDR)授权的公告机构查询地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34
3.欧盟个人防护装备条例EU2016/425(PPE)授权的公告机构查询地址:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=155501
二、美国对口罩等防疫用品准入要求
(一)口罩
美国对医用口罩和防护口罩同样区分管理,其中医用口罩由美国食品药品监督管理局(FDA)管理,而个人防护口罩则由美国国家职业安全卫生研究所(NIOSH)管理。
1. 医用口罩
医用口罩需通过FDA注册,企业直接向FDA官网申请并提交相关材料。此外还有两种可选途径:
(1)已经获得NIOSH注册的N95口罩,在产品生物学测试、阻燃测试和血液穿透测试通过的情况下,可以豁免产品上市登记(510K),直接进行FDA工厂注册和医疗器械列名。
(2)如果获得持有510K的制造商的授权,可以作为其代工厂使用其510K批准号进行企业注册和器械列名。
2. 个人防护口罩
防护口罩需通过NIOSH注册,企业直接在NIOSH官网申请。
(二)防护服
对医用防护服和个人防护服的管理也类似于口罩的管理方式,其中医用防护服由美国食品药品监督管理局(FDA)管理,而个人防护服由美国国家职业安全卫生研究所(NIOSH)管理。企业直接在FDA或NIOSH进行注册申请。